La rivière borde mon terrain, elle est publique évidemment, le talus entre la rivière et ma haie aussi par contre c’est chiant à entretenir par la commune du coup ça n’est jamais fait ..
Je mets les bottes 3 fois par ans pour débroussailler et nettoyer en faisant attention aux périodes de reproduction
C’est sympa d’avoir poules d’eau colverts sarcelles et Martins pêcheurs ![]()
Pourquoi penses-tu qu’aucun boinsaika n’ai fait d’analyse ? Certains sont des professionnels maraîchers, horti avec un bagage d’études et de pratiques élevés. Ils gèrent leurs apports d’eau et d’engrais de façon automatisé avec une grande precision et des résultats concrets sur un grand nombre de bonsaï, et cela depuis des années. Leurs expériences est accessible. Comment peux tu affirmer que certains clubs ne federent pas leurs achats et certaines analyses? D’eau, maladie crypto… pour cela il faut adhérer à un club.
Je pense qu’il est urgent de vérifier ce que tu affirmes. D’une part, les distributeurs d’eau doivent assurer un pH de l’eau supérieur à 6,5 pour éviter la corrosion des conduites métalliques. Donc, en région cristalline, c’est pas difficile l’eau du réseau est plus dure celle des pompages. Il y a une autre raison : quand les sous-sols sont cristallins, la porosité est globalement faible, ce qui, dès que la population est un peu dense, oblige à prélever dans les eaux de surface, fortement chargées en matière organique, que l’on fait floculer à la chaux, ce qui lui donne ispo facto un pH et une dureté bien plus importantes.
Ta carte est fausse. Par exemple je suis dans les Landes et leau du forage qui est distribué dans mon réseau est une résurgence dune rivière souterraine, qui vient du massif central. Qui a la même composition que leau d’evian. Une eau tres dure et alcaline. A 2km c’est une eau de source très douce… mais tout cela est peu important. Les cultures hors sol, pour rester sur le bonsai, avec le même substrat, le même mode de culture, les mêmes essences on ne voit pas de différence de croissance. Je pense que sur ce forum et une grande majorité de bonsaika ne se prennent pas la tête avec la composition de leur eau. Ils ont pourtant d’excellents résultats aussi.
Faut que tu cherches des indices de présence de la Loutre sur ta rivière. Tu vas voir, les crottes sentent très bon.
je ne suis pas chimiste, ou plutot un chimiste du Dimanche, mais voilà ce que j’avais obtenu avec mon kit “Control-TH” réalisé il y a qcq années, lorsque j’arrosais avec l’eau du puits.
eau du robinet = 50gouttes (1 goutte correspond à 10mg/L de calcium)
eau du puits = 24 gouttes
eau du puits préalablement acidifiée à PH6 = 24 gouttes
→ d’où ma conclusion que la dureté est la même sans et avec PHdown
d’autres mesures, pour le fun :
eau adoucie = 11 gouttes
eau de pluie récoltée sur les dalles = 4 gouttes
eau déminéralisée = 0 goutte (ça me parait logique)
eau de source “pas du houx” = 3 gouttes ( = parfait : c’est cette eau que j’utilise quand je n’ai plus d’eau de pluie)
eau de source cristalline = 25 gouttes (trop élevé pour une utilisation Bonsai)
eau de pluie issue du toit avec gouttière remplie de feuilles mortes (couleur jaunatre, 3 gouttes, PH6.5) → parfait pour l’arrosage des arbres
eau de pluie issue du toit avec gouttière propre (1 goutte, PH compris en 6,5 et 7) → parfait pour les arbres
je te conseille de trouver une eau de source avec 20, 30 ou 40 mg/L de calcium et PH = 6 ou 7 mais le mieux est de récolter l’eau de pluie (economique, compo parfaite)
Pas chez moi, eau du robinet = 50 gouttes (donc 50 °f donc 500 mg/L de calcium), eau du puits = 24 gouttes (donc 2 fois moins)
Je parlais d’analyse sol. Il se trouve que c’est celui ci qui est l’habitat des racines et du plant, et que lesprojections depuis l’eau et les engrais sont imparfaites. Qui fait des analyses sols en bonsai ?
Ca tombe bien, j’ai dit qu’elle était assez fausse, et ue toute situation individuelle pouvait s’en écarter.
Avant de t’opposer pour t’opposer et par posture, tu peux aussi lire ( avant ).
Je parlais de généralité ( et donc une majorité assez large des cas en bassin de population ).
Je parlais dureté et tu enchaines sur le pH.
Factuellement, dans énormément de bassin d’eau réseau, il y a une part de forage profond ( peu dur ) et une part d’eau de surface / de captage ( trés vrariable selon le coin ). Dans énormément de cas, et sans doute 70 / 80 % de la population concernée, le réseau est porté par une eau moins dure qu’en surface car en partie de forage. Des exemples personnels sont des illustration diverses le cas échéant, mais ne font pas une tendance majoritaire ou presque hégémonique.
Enfin, et je radote, la relation dureté et pH n’est pas une évidence sur une source ponctuelle ( profonde ou de surface ).
J’ai cité Sainte Anne Abatilles ( et presque la même chose pour l’eau de réseau du sud bassin, qui est assez proche puisqu’en bonne partie issu d’un forage similaire - le complément en eau de surface dépend de captages de surfaces en milieu sables, donc assez proches en fait ). pH supérieur à 8 ( clairement basique ) et dureté inférieure à 10 ( donc clairement une eau trés « douce » ). Ca parait antinomique, et finalement ca ne l’est pas forcément.
Mais dans tous les cas, si on acidie cette eau, on aura encore moins de calcium ( et là, vraiment trés trés peu pour du végétal ).
Tu es sûr de ça ?
Il m’a fallu le même nombre de gouttes (24) pour mon eau du puits sans PHdown et avec PHdown. Autrement dit, l’acidification de mon eau du puits n’a pas changé sa dureté (24gouttes = 24 °f = 240mg/L de calcium) ou alors ça se joue à 1/2 goutte ? ![]()
J’ai bien compris que tu parlais d’analyse de sol.faut arrêter de prendre tout le monde de haut. Et oui j’en connais qui en font pour corriger leur apports d’engrais. Pour vérifier si leurs projections sonr bonnes. Malheureusement et ue fois de plus, ru parle de théories et non de cas concret.
Évidemment, parce que le pH est remonté en rajoutant du carbonate de calcium…Par ailleurs, l’idée que les eaux de forages seraient moins minéralisées que les eaux de surface, c’est vraiment n’importe quoi. Les eaux des nappes aquifères se mettent en équilibre avec la roche dans lesquelles elles sont placées, si c’est un calcaire, elles deviennent très calcaires, si c’est un autre type de roche, elles prennent d’autres ions.
J’aimerais tester la dureté de mon eau du robinet , la marque JBL propose des tests KH ou GH lequel dois-je prendre selon vous ?
Merci
Pour faire simple, le test GH c’est pour connaître la dureté totale de l’eau, il se base essentiellement sur les ions de calcium et magnésium, le KH c’est pour connaître la dureté carbonatée, donc basé sur les carbonates et bicarbonates.
Le test GH est plus souvent pour l’aquariophilie d’eau douce, et le KH pour les aquariums marins.
Dans ton cas le test GH suffira.
Maintenant si tu veux connaître la valeur exacte de calcium dans ton eau JBL fait aussi les test CA .
perso j’ai utilisé ce test, sans trop me poser de question sur sa fiabilité vu qu’il s’agit de réactifs ![]()
le modèle vendu actuellement est dans une boite en carton, alors que le mien était dans un coffret en plastic noir mais c’est juste du packaging. Il est fabriqué en France
Ton fournisseur d’eau est censé communiquer chaque année l’analyse précise et complète de l’eau qu’il délivre ![]()
Il faut y voir deux avantages, en premier c’est gratuit et en second cela évite de se prendre la tête avec des calculs alambiqués et des avis divergents ![]()
Merci pour le conseil fabizen et gp1 !
J’ai trouvé ça en 5mn ! voilà l’analyse , du coup qu’en pensez vous ?
Merci !
Autant que 1+1 = qq chose proche de 2, dans un monde normal.
Je vais essayer de pas trop disperser, mais un minimum est nécessaire.
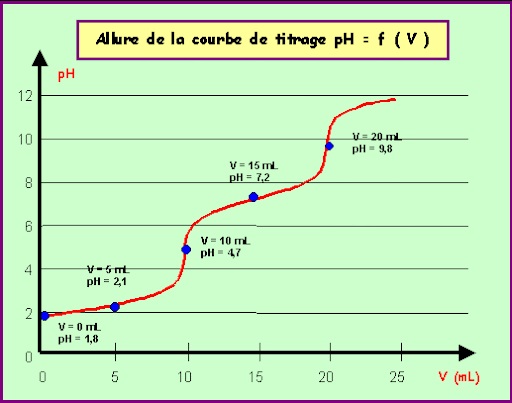
1) la correction du pH n’est pas linéaire.
Ceci est la courbe de dosage d’acide phosphorique avec de la soude( probabilité raisonnable que ce soit le constituant de ton pH down ). Bon ici, c’est l’ajout de soude ( le volume est en ml et pas en goutte sur l’axe hoizontal ) et pas de l’acide dans l’eau, qui sera une courbe inversée, mais la typologie reste identique.
Il y a des phases de paliers ( le pH joue peu avec 20 % de gouttes en plus ou en moins ) et des phases de transition plus abruptes. La stabilité se joue autour des pKa, et c’est trés instable entre les 2 ( ici la zone instable entre pH 3 et pH 6 soit autour de 4.7 )
2) Si on en restait à celà ce serait trop simple et il n’y aurait pas débat.
Ca++ et CaCO3.
Dans l’eau il y a du Ca++ libre comme Max ( il est libre Max ) et du CaCO3 ( du calcaire ). Le calcaire est quasi insoluble, mais avant d’être d’être une stalagtite visible ou un gros pavé qui sédimente vite, il y a les cristaux insolubles mais qui sont sont sujets au « remuage » de la solution. Donc il faut considérer 2 choses en parallèle. Ca++ ET CaCO3.
Ca++:
A chaque goutte d’acide, alors l’acide ( phosphorique ou sulfurique ou chlorydrique ou organique ) va capter un Ca++ pour former un sel précipitant assez largement, ça libère un proton H+, ça acidifie en mesure. Et à chque fois, ça fait un Ca++ qui disparait pour la mesure de dureté « vraie » et pour l’assimilation vers la CEC du sol, donc non assimilable par la plante.
CaCO3
A chaque acidification, il y a un phénomène inverse ( partiel ) sur ces micro cailloux de calcaire ( qu’on ne voit pas, en suspension dans l’eau ). L’acidification conduit à une remise dans le milieu de Ca++. C’est comme ça qu’on teste une roche ( sous acide chlorydrique ) quand ça mousse c’est bien du calcaire. C’est aussi le phénomène qui « abime » le calcaire sous divers composés, comme HCO3-, et qui en font une roche fragile et altérable.
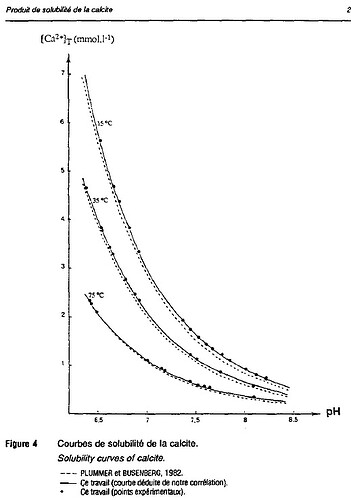
Voir ce graphe par exemple, la solubilité de la calcite ( calcaire CaCO3 ) en fonction du pH.
Et il y a l’impact température ! ( introduit aussi par le graphe au dessus ).
Pourquoi y’a du calcaire sur la résistance d’un chaufgfe eau, dans un bouilleur d’eau, ou préférentiellement sur l’extérieur arrivée eau chaude dans la douche ? La température…
Ce n’est pas forcément anodin en été quand la source d’eau est à 15° constant ( eau réseau ou eau puit ) et se retrouve à 30° en qq minutes / heures.
L’ensemble des phénomènes est lié des points d’équilibres, qui seront atteints si on laisse le temps, mais parfois une mesure trop rapide peut induire vers l’erreur. Ca dépend aussi d’une question de cinétique des réactions.
Un exemple qui demande du temps long, c’est l’apport du CO2 atmosphérique à l’interface d’un bac rempli d’eau et à l’air libre.
Sur un temps LONG, l’eau de l’arrosoir tendra vers une pression CO2 dissout constant dans l’eau, et vers l’équilibre avec la pCO2 de l’air. Donc une eau à l’air libre tendra vers 400 mg/l ( la flemme de refaire les calculs, c’est un ordre de grandeur ) de H+CO3-. Donc cette eau sera légèrement « pétillante » même si le palais le le détecte pas ( sa limite de détection sera au dessus du gramme ). Mais une eau souterraine sera acidifiée, et « carbonatée » dans le sens la « bulle »
Dans la mesure personnelle avec des outils trés perfectibles, il y a une somme de points d’erreu de mesure qui arrivent à ..ne pas pouvoir conclure grand chose. Les conditions de T°, de pression, de temps, de l’eau de base, de la qualité du test, etc…On peut s’amuser avec ça, mais ce sera souvent un grand cirque.
@lanig
Factuellement, les eaux de forage viennent essentiellement de roches plus anciennes que la surface, et sauf exceptions RARES seront plus riches en milieu siliceux / cristallin que des eaux de surface. Par définition aussi, on trouvera BIEN plus souvent des calcaires en surface, sur des puits de surface.
Les eaux de captation sont par nature ULTRA hétérogènes, de assez neutre ( étang et retenue de pluviométrie ) à assez basique en zone calcaire, parfois ( rarement ) acides en zones siliceuses ou cristallines en général.
J’ai parlé de généralité, tu cherches à ériger des exceptions en généralité / majorité, ce qui est pas bien loin de la malhonneteté.
@Marc40
Je parle de théorie ?
Emile Clapeyron a écrit la loi des gaz parfaits en 1834. Il maitraisait les unités dont il parlait, liste ( non exhaustive ) la pression, le volume, le nb d’avogadro, la mole, la température absolue. Personne ne l’a remis en cause, c’est un fondement de la « science » moderne et toujours viable. Tout au plus, on a connaissances des approximations de cette loi sur des cas rares ( gaz lourd à trés haute pression à titre d’exemple ).
Entre 1908 et 1916, Henderson puis Hasselbach ont donné ont « maitrisé » la notion de l’équation du pH dans un milieu tamponné, avec la notion de constante d’acidité. En 2026, ça reste tellement vrai que personne n’a eu l’ombre d’un soupçon de début de chance d’y trouver à redire . Ces 2 notions sont en apprentissage entre la fin du lycée ( en approche superficielle avec les options sciences ) et la fin de 2eme année de cycle sup en étude science. C’est juste une base ( l’alphabet ) , ensuite l’apprentissage se porte sur des choses plus fines et plus spécialisées.
Abscence de mise en pratique, so what ? Qui a ICI une analyse de substrat EN SITUATION dans un pot en culture, depuis 6 mois, puis la même à 3 ans, en ayant les paramètres connus ( identifiés et connus ) de l’engrais et de l’eau ? Personne !!! ( moi non plus ).
L’acharné de l’engrais pensera que celui fait tout et régit tout ( y compris le pH ).
L’acharné de l’eau pensera que cellle ci…Bla bla vous avez compris.
L’acharné du substrat pensera…Bla bla.
La réalité est un mix des 3.